
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
Masse de Cu en grammes peut être obtenu en multipliant le Masse en amu avec le numéro d'Avogadro. Par conséquent, la masse de 3,5 moles de Cu est de 3,69 × 10−22 grammes 3,69 × 10 − 22 grammes.
En conséquence, quelle est la masse d'une mole de cuivre ?
La relation entre moléculaire (formule) Masse et molaire Masse • Pour en obtenir un mole de cuivre atomes (6,02 x 1023 atomes), peser 63,55 g le cuivre . La molaire Masse (M) d'une substance est le Masse d'un Môle des entités (atomes, molécules ou unités de formule) de la substance.
A côté ci-dessus, quelle est la masse en grammes de 3,2 moles de cuivre Cu ? 203,36 grammes
Alors, combien y a-t-il de grammes dans 3,35 moles de cuivre ?
1 Môle est égal à 1 taupes Cuivre , ou 63,546 grammes.
Combien de moles y a-t-il dans un gramme ?
Nous supposons que vous effectuez la conversion entre taupes Dans et gramme . Vous pouvez afficher plus de détails sur chaque unité de mesure: poids moléculaire de In ou grammes L'unité de base SI pour la quantité de substance est la Môle . 1 Môle est égal à 1 taupes Dans, ou 114.818 grammes.
Conseillé:
Quel est le rapport entre les moles d'eau et les moles de CuSO4 ?

Divisez le nombre de moles d'eau perdues par le nombre de moles de sel anhydre pour obtenir le rapport des molécules d'eau aux unités de formule. Dans notre exemple, 0,5 mole d'eau ÷ 0,1 mole de sulfate de cuivre = rapport 5:1. Cela signifie que pour chaque unité de CuSO4 présente, nous avons 5 molécules d'eau
Quelle est la structure cristalline du sulfate de cuivre ?

Sulfate de cuivre(II) Noms Structure Structure cristalline Orthorhombique (anhydre, chalcocyanite), groupe spatial Pnma,oP24, a = 0,839 nm, b = 0,669 nm, c = 0,483 nm. Triclinique (pentahydraté), groupe d'espace P1, aP22, a = 0,5986 nm, b = 0,6141 nm,c = 1,0736 nm, α = 77,333°, β = 82,267°, γ= 72,567° Thermochimie
Quelle est la formule du séléniure de cuivre II ?

Propriétés du séléniure de cuivre(II) (théorique) Formule du composé CuSe Densité 5,99 g/cm3 Solubilité dans H2O N/A Masse exacte 142,846119 g/mol Masse monoisotopique 142,846119 g/mol
Quelle est la différence entre la masse d'un proton et la masse d'un électron ?
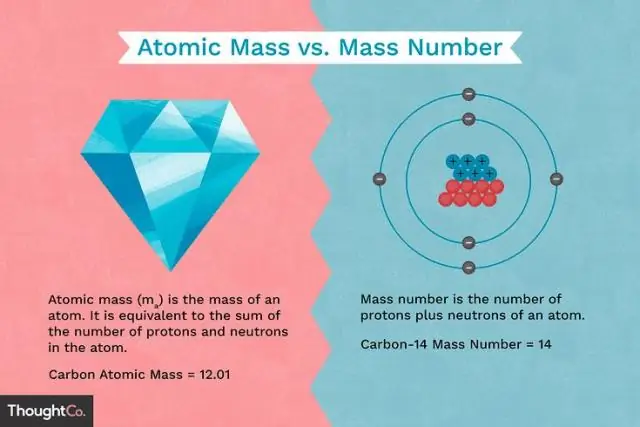
Les protons et les neutrons ont approximativement la même masse, mais ils sont tous les deux beaucoup plus massifs que les électrons (environ 2 000 fois plus massifs qu'un électron). La charge positive sur un proton est égale en amplitude à la charge négative sur un électron
Quelle est la composition en pourcentage de cuivre et de brome dans CuBr2 ?

Composition en pourcentage par élément Symbole de l'élément Masse Pourcentage de cuivre Cu 28,451% Brome Br 71,549%
