
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
Il considère également leur physique simple Propriétés comme la solubilité et les points d'ébullition. Aldéhydes et cétones sont des composés simples qui contiennent un groupe carbonyle - une double liaison carbone-oxygène.
Justement, quelles sont les propriétés physiques des cétones ?
Propriétés physiques d'aldéhydes et Cétones : Point d'ébullition: Le point d'ébullition du méthanal est de -19o C et pour l'éthanal c'est +21o C. De cela, nous pouvons dire que le point d'ébullition de l'éthanal est proche de la température ambiante. En général, le point d'ébullition des aldéhydes et cétones augmente avec l'augmentation du poids moléculaire.
quelles sont les utilisations des cétones ? Utilisations des cétones La cétone se comporte comme un excellent solvant pour certains types de plastiques et de fibres synthétiques. L'acétone agit comme un diluant pour peinture et un dissolvant pour vernis à ongles. Il est également utilisé à des fins médicinales telles que la procédure de peeling chimique ainsi que acné traitements.
A côté de ci-dessus, quelles sont les propriétés des aldéhydes et des cétones ?
Propriétés des aldéhydes et des cétones Aldéhydes et cétones peut former de faibles liaisons hydrogène avec l'eau à travers l'atome d'oxygène carbonyle. Les membres inférieurs des deux séries (3 carbones ou moins) sont solubles dans l'eau en toutes proportions. Au fur et à mesure que la longueur de la chaîne carbonée augmente, la solubilité dans l'eau diminue.
Quelles sont les propriétés des aldéhydes ?
La polarité du groupe carbonyle affecte notamment la physique Propriétés du point de fusion et du point d'ébullition, de la solubilité et du moment dipolaire. Les hydrocarbures, composés constitués uniquement des éléments hydrogène et carbone, sont essentiellement non polaires et ont donc des points de fusion et d'ébullition bas.
Conseillé:
Quelles sont les propriétés des mathématiques et des exemples ?

Il y a quatre propriétés mathématiques qui impliquent l'addition. Les propriétés sont les propriétés commutatives, associatives, additives d'identité et distributives. Propriété d'identité additive : la somme de n'importe quel nombre et de zéro est le nombre d'origine. Par exemple 5 + 0 = 5
Quelles propriétés sont des exemples de propriétés chimiques cochez toutes celles qui s'appliquent ?

Des exemples de propriétés chimiques comprennent l'inflammabilité, la toxicité, l'acidité, la réactivité (de nombreux types) et la chaleur de combustion. Le fer, par exemple, se combine avec l'oxygène en présence d'eau pour former de la rouille; le chrome ne s'oxyde pas (Figure 2)
Quelles sont les trois propriétés que les astronomes utilisent pour décrire les étoiles ?

Une étoile peut être définie par cinq caractéristiques de base : luminosité, couleur, température de surface, taille et masse. Luminosité. Deux caractéristiques définissent la luminosité : la luminosité et la magnitude. Couleur. La couleur d'une étoile dépend de sa température de surface. Température de surface. Taille. Masse
Lesquelles des propriétés suivantes sont toutes des propriétés physiques de la matière ?
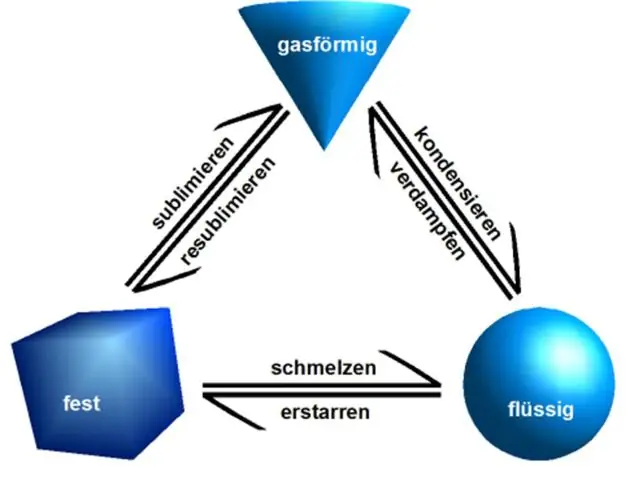
Propriétés physiques : Les propriétés physiques peuvent être observées ou mesurées sans modifier la composition de la matière. Les propriétés physiques comprennent : l'apparence, la texture, la couleur, l'odeur, le point de fusion, le point d'ébullition, la densité, la solubilité, la polarité et bien d'autres
Les cétones ou les aldéhydes ont-ils des points d'ébullition plus élevés ?

Pour les cétones et les aldéhydes de masse moléculaire similaire, les cétones ont un point d'ébullition plus élevé en raison du fait que son groupe carbonyle est plus polarisé que dans les aldéhydes. Ainsi, les interactions entre molécules de cétones sont plus fortes qu'entre molécules d'aldéhydes, et cela donne un point d'ébullition plus élevé
