
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
Éléments diatomiques sont tous des gaz, et ils forment molécules parce qu'ils n'ont pas de coques à valence complète par eux-mêmes. Les éléments diatomiques sont: le brome, l'iode, l'azote, le chlore, l'hydrogène, l'oxygène et le fluor. Les moyens de s'en souvenir sont: BrINClHOF et Have No Fear Of Ice ColdBeer.
A côté de cela, quels éléments sont dans la nature en tant que molécules diatomiques ?
Ils sont sept éléments cette naturellement se produire comme homonucléaire molécules diatomiques dans leurs états gazeux: hydrogène, azote, oxygène, fluor, chlore, brome et iode.
Sachez également pourquoi le chlore se présente-t-il sous forme de molécule diatomique dans la nature ? Avec sept électrons sur son orbite la plus externe - un électron en deçà d'un "huit stable" - l'élément chlore existe dans la nature comme un molécule diatomique . Cet arrangement permet à deux chlore atomes de partager leurs électrons de l'orbite la plus externe, obtenant ainsi une stabilité par rapport à l'atome unique.
De celui-ci, qu'est-ce qu'un élément diatomique ?
A température ambiante, il y a cinq éléments diatomiques , qui existent tous sous forme gazeuse: hydrogène, azote, oxygène, fluor et chlore. Si la température est légèrement augmentée, deux autres éléments seront présents: brome et iode.
Comment se forment les molécules diatomiques ?
Diatomique Éléments Les éléments qui forment deux atomes molécules à température ambiante sont l'hydrogène, l'azote, l'oxygène et les halogènes fluor, chlore, brome et iode. L'azote se distingue parce que ses atomes partagent une triple liaison forte, ce qui en fait une substance très stable.
Conseillé:
Où se trouvent certains des volcans les plus célèbres ?

Top 10 des volcans les plus célèbres du monde Krakatoa, Indonésie. Mont Etna, Italie. MAUNA LOA, Hawaï. Mont Fuji, Tokyo. Mont Pinatubo, Philippines. Mt. Pelée, Martinique. Mont Tambora, Indonésie. Mont Cotopaxi, Amérique du Sud
Pourquoi certaines roches ignées extrusives se trouvent-elles sous terre ?

Sommaire. Les roches ignées intrusives se refroidissent lentement du magma parce qu'elles sont enfouies sous la surface, elles ont donc de gros cristaux. Les roches ignées extrusives se refroidissent rapidement à partir de la lave car elles se forment à la surface, elles ont donc de petits cristaux
Comment écrivez-vous sous forme de fraction sous la forme la plus simple ?
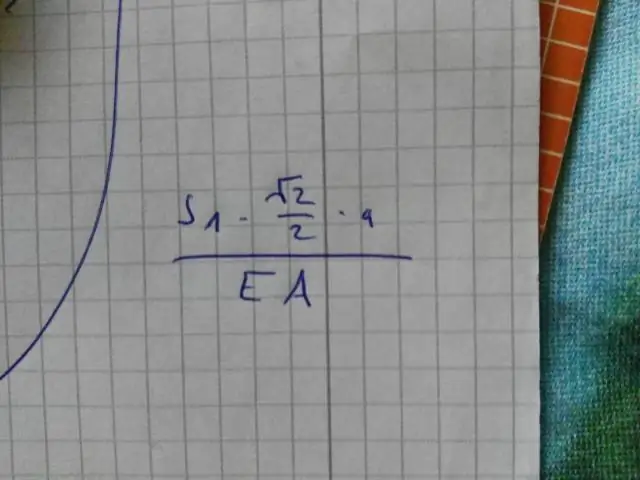
Lors de l'écriture des fractions sous la forme la plus simple, il y a deux règles à suivre : Demandez si le numérateur et le dénominateur peuvent être divisés par le même nombre, qui est appelé un facteur commun. Voir si au moins un nombre dans la fraction est un nombre premier
Comment l'oxygène se produit-il dans la nature et explique-t-il le cycle de l'oxygène dans la nature ?

Expliquer le cycle de l'oxygène dans la nature. L'oxygène existe sous deux formes différentes dans la nature. Ces formes se présentent sous forme d'oxygène gazeux à 21 % et se combinent sous forme d'oxydes de métaux et de non-métaux, dans la croûte terrestre, l'atmosphère et l'eau. L'oxygène est renvoyé dans l'atmosphère par le processus appelé photosynthèse
Pourquoi les molécules diatomiques sont-elles importantes ?

Les éléments diatomiques ont joué un rôle important dans l'élucidation des concepts d'élément, d'atome et de molécule au XIXe siècle, car certains des éléments les plus courants, tels que l'hydrogène, l'oxygène et l'azote, se présentent sous forme de molécules diatomiques
