
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-06-01 05:04.
deux
De ce fait, quels éléments sont des exceptions au principe Aufbau ?
Par exemple, le ruthénium, le rhodium, l'argent et le platine sont tous exceptions au principe Aufbau à cause des sous-coques remplies ou à moitié remplies.
A côté de ci-dessus, pourquoi la configuration électronique pour le cuivre est-elle 1s22s22p63s23p63d104s1 au lieu de 1s22s22p63s23p63d94s2 ? Un sous-niveau rempli est plus stable qu'un sous-niveau à moitié rempli. L'agencement de électrons avec le même spin est aussi petit que possible. L'orbitale 4s a une énergie plus élevée que l'orbitale 3d.
Également demandé, comment écrivez-vous la configuration électronique pour les éléments du bloc D ?
Généralement, le configuration électronique de ces éléments est (n-1) ré 1-10ns 1-2. Le (n-1) reste pour l'intérieur ré les orbitales qui peuvent avoir un à dix électrons et l'orbitale ns périphérique peut avoir un ou deux électrons. Les ré - bloquer implique la zone médiane flanquée de s- et p- blocs dans le tableau périodique.
Pourquoi Cr et Cu présentent-ils une configuration irrégulière ?
La même chose arrive avec Cu . Nous pouvez voir ça dans Cu La sous-couche d a 9 électrons, donc pour devenir stable, il faut 1 électron de plus dans la sous-couche d, il faudra donc 1 électron à la sous-couche s et maintenant Cu deviendra stable dans sa nouvelle électronique configuration . D'où, Cr et Cu sont dit exceptionnel configuration.
Conseillé:
Comment la théorie cinétique de la matière se rapporte-t-elle aux solides, aux liquides et aux gaz ?

La théorie moléculaire cinétique de la matière stipule que : La matière est composée de particules qui se déplacent constamment. Toutes les particules ont de l'énergie, mais l'énergie varie en fonction de la température à laquelle se trouve l'échantillon de matière. Cela détermine à son tour si la substance existe à l'état solide, liquide ou gazeux
Combien y a-t-il de chauves-souris dans la grotte aux cerfs de Bornéo ?

Au crépuscule, un essaim de chauves-souris se disperse pour chasser dans la forêt tropicale entourant Deer Cave. L'un des plus grands passages souterrains de la planète, il abrite plus de deux millions de chauves-souris
Quels niveaux de grossissement peuvent être atteints par les microscopes optiques par rapport aux microscopes électroniques ?
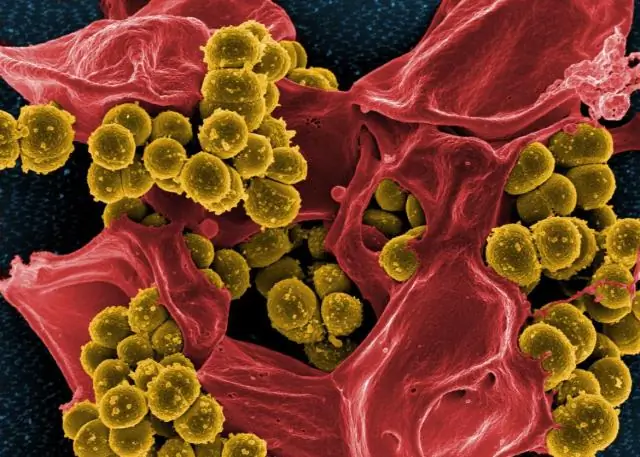
Un microscope électronique à transmission à balayage a atteint une résolution supérieure à 50 pm en mode d'imagerie annulaire sur fond noir et des grossissements allant jusqu'à environ 10 000 000 × alors que la plupart des microscopes optiques sont limités par la diffraction à une résolution d'environ 200 nm et des grossissements utiles inférieurs à 2000 ×
Comment se comparent les configurations électroniques au sein d'un même groupe d'éléments ?

Comment se comparent les configurations électroniques au sein d'un même groupe d'éléments ? Les éléments d'un même groupe ont les mêmes configurations d'électrons de valence. Cela signifie qu'ils ont complètement rempli les sous-niveaux s et p, ce qui leur donne un "octet stable" d'électrons dans leur niveau externe
Les humains sont-ils plus étroitement liés aux gorilles ou aux orangs-outans ?

Pour la plupart des séquences d'ADN, les humains et les chimpanzés semblent être les plus étroitement liés, mais certains indiquent un clade humain-gorille ou chimpanzé-gorille. Le génome humain a été séquencé, ainsi que le génome du chimpanzé. Les humains ont 23 paires de chromosomes, tandis que les chimpanzés, les gorilles et les orangs-outans en ont 24
