
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
Atomique spectre d'émission proviennent des électrons passant de niveaux d'énergie supérieurs à des niveaux d'énergie inférieurs dans le atome , des photons (paquets lumineux) avec des longueurs d'onde spécifiques sont libérés.
Justement, qu'est-ce qui cause le spectre d'émission?
Ainsi, spectre d'émission sont produits par des gaz minces dans lesquels les atomes ne subissent pas beaucoup de collisions (à cause de la faible densité). Les émission les lignes correspondent à des photons d'énergies discrètes qui sont émis lorsque les états atomiques excités dans le gaz font des transitions vers des niveaux inférieurs.
pourquoi le spectre d'émission est-il unique pour chaque élément ? Spectre d'émission de chaque élément est distinct parce que chaque élément a un ensemble différent de niveaux d'énergie des électrons. Les émission les lignes correspondent aux différences entre les différentes paires des nombreux niveaux d'énergie. Les lignes (photons) sont émis à mesure que les électrons tombent des orbitales à haute énergie vers des énergies plus basses.
Par conséquent, comment est produit un spectre d'émission atomique d'un élément ?
Un spectre d'émission atomique est le motif des lignes formé lorsque la lumière passe à travers un prisme pour le séparer en différentes fréquences de lumière qu'il contient. De même, lorsque le atomes détendu à un état d'énergie inférieur, n'importe quelle quantité d'énergie pourrait être libérée.
Pourquoi le spectre d'émission d'un élément est-il considéré comme son empreinte ?
Atomique spectre d'émission sont uniques spectres de la lumière émis par un élément lorsque l'électricité y passe ou lorsqu'elle est vue à travers un prisme. Parce qu'ils sont uniques, ils peuvent agir comme un élément s empreinte digitale . C'est un ensemble de fréquences de les électromagnétique spectre émis par excité éléments d'un atome.
Conseillé:
Quelles sont les causes des raies dans le spectre d'émission des éléments ?

Les raies d'émission se produisent lorsque les électrons d'un atome, d'un élément ou d'une molécule excités se déplacent entre les niveaux d'énergie, retournant vers l'état fondamental. Les raies spectrales d'un élément ou d'une molécule spécifique au repos dans un laboratoire se produisent toujours aux mêmes longueurs d'onde
En quoi un spectre d'émission atomique est-il différent d'un spectre continu ?

Spectre continu : un spectre qui a toutes les longueurs d'onde sans lacunes sur une large plage. Spectre d'émission : lorsqu'un électron dans un état excité passe à un niveau d'énergie inférieur, il émet une certaine quantité d'énergie sous forme de photons. Le spectre de cette transition est constitué de raies car les niveaux d'énergie sont quantifiés
Le spectre d'émission atomique est-il une gamme continue de couleurs ?

T/F Comme le spectre visible, un spectre d'émission atomique est une gamme continue de couleurs. T/F Chaque élément a un spectre d'émission atomique unique. V/F Le fait que seules certaines couleurs apparaissent dans le spectre d'émission atomique d'un élément indique que seules certaines fréquences de lumière sont émises
Pourquoi le spectre d'absorption de la chlorophylle a et le spectre d'action de la photosynthèse sont-ils différents ?
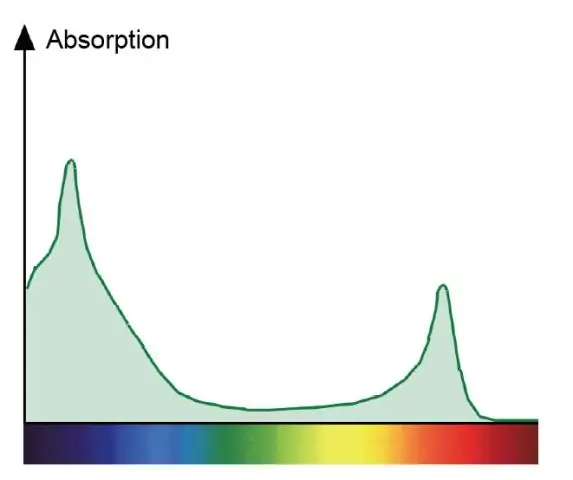
Un spectre d'absorption montre toutes les couleurs de la lumière absorbée par une plante. Un spectre d'action montre toutes les couleurs de la lumière qui sont utilisées dans la photosynthèse. Les chlorophylles sont les pigments verts qui absorbent le rouge et le bleu et participent directement à la photosynthèse
Quel est le spectre d'émission du soleil ?

Le spectre d'émission du Soleil. Le Soleil émet un rayonnement électromagnétique sur une large gamme de longueurs d'onde. Le maximum dans le spectre d'émission solaire se situe à environ 500 nm, dans la partie bleu-vert du spectre visible. En plus de la lumière visible, le Soleil émet un rayonnement ultraviolet et un rayonnement infrarouge
