
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
Lorsque vous changez les coefficients , tu 'seulement changer le nombre de molécules de cette substance particulière. Cependant, quand vous changez les indices , tu es changer la substance elle-même, ce qui volonté faire votre équation chimique tort.
De même, pourquoi les indices ne peuvent-ils pas changer lors de l'équilibrage d'une équation chimique ?
Seuls les coefficients peuvent être modifié afin de équilibrer une équation chimique . Indices font partie du formule chimique pour les réactifs ou les produits et ne peut pas être modifié à équilibre un équation . En changeant une changements d'indice la substance représentée par le formule.
Aussi, pourquoi utilise-t-on des coefficients pour équilibrer les équations ? Dans un équilibré chimique équation , le nombre total d'atomes de chaque élément présent est le même des deux côtés du équation . Stoechiométrique coefficients sont les coefficients nécessaire pour équilibre un produit chimique équation . Celles-ci sont importantes car elles relient les quantités de réactifs utilisé et les produits formés.
A savoir aussi, pourquoi est-il important de réduire les coefficients dans une équation équilibrée au plus bas possible ?
La réponse est: c'est important parce que de cette façon le chimiste peut voir le plus bas possible nombre de réactifs dans chimique réaction nécessaire pour former le produit de la réaction. Coefficients avec le le plus bas rapport indiquent les quantités relatives de substances dans une réaction.
Que peut-on ajuster lors de l'équilibrage des équations chimiques ?
Lorsque vous équilibre un équation tu pouvez ne changez que les coefficients (les nombres devant les molécules ou les atomes). Les coefficients sont les nombres devant la molécule. Les indices sont les plus petits nombres trouvés après les atomes. Ceux-ci ne peuvent pas être changé lors de l'équilibrage des équations chimiques !
Conseillé:
Quels sont les trois types d'équations chimiques ?

Les types de réactions chimiques les plus courants sont les suivants : Combinaison. Décomposition. Déplacement unique. Double déplacement. La combustion. Redox
Que sont les symboles chimiques et les formules chimiques ?
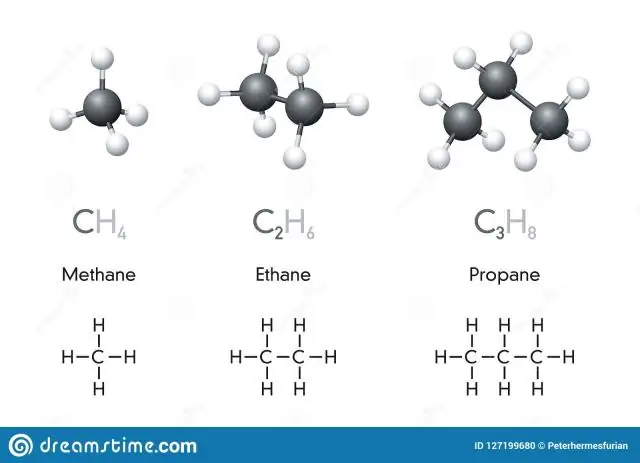
Un symbole chimique est une désignation en une ou deux lettres d'un élément. Les composés sont des combinaisons de deux éléments ou plus. Une formule chimique est une expression qui montre les éléments d'un composé et les proportions relatives de ces éléments. De nombreux éléments ont des symboles qui dérivent du nom latin de l'élément
Que vous disent les coefficients d'une équation chimique équilibrée sur les réactifs et les produits ?

Les coefficients d'une équation chimique équilibrée nous indiquent le nombre relatif de moles de réactifs et de produits. Pour résoudre des problèmes stoechiométriques, des facteurs de conversion reliant les moles de réactifs aux moles de produits sont utilisés. Dans les calculs de masse, la masse molaire est nécessaire pour convertir la masse en moles
Comment équilibrer les équations chimiques avec les nombres d'oxydation ?

Dans la méthode du nombre d'oxydation, vous déterminez les nombres d'oxydation de tous les atomes. Ensuite, vous multipliez les atomes qui ont changé par de petits nombres entiers. Vous faites en sorte que la perte totale d'électrons soit égale au gain total d'électrons. Ensuite, vous équilibrez le reste des atomes
Lors de l'équilibrage d'une équation chimique, vous ne pouvez que changer ?

Lorsque vous équilibrez une équation, vous ne pouvez modifier que les coefficients (les nombres devant les molécules ou les atomes). Les coefficients sont les nombres devant la molécule. Les indices sont les plus petits nombres trouvés après les atomes. Ceux-ci ne peuvent pas être modifiés lors de l'équilibrage des équations chimiques
