
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
UNE sel hydraté est un cristallin sel molécule qui est lâchement attachée à un certain nombre de molécules d'eau. Le sel est créé lorsqu'un anion d'acide et un cation de base sont combinés pour produire une molécule acide-base. Dans un sel hydraté , les molécules d'eau sont incorporées dans la structure cristalline du sel.
Les gens demandent également, quels sont les sels hydratés, donnez des exemples ?
D'autres exemples d'hydrates sont le sel de Glauber ( sulfate de sodium décahydraté, Na2DONC410H20); cristaux de soude ( sodium carbonate décahydraté, Na2CO310H20); borax ( sodium tétraborate décahydraté, Na2B4O710H20); les sulfates connu sous le nom de vitriols (par exemple, sel d'Epsom, MgSO47H20); et les sels doubles connus collectivement sous le nom d'alun (M+2
Par la suite, la question est, quelle est la différence entre le sel hydraté et le sel anhydre ? Différence entre le sel hydraté et le sel anhydre . La clé différence entre sel hydraté et sel anhydre est-ce le sel hydraté les molécules sont attachées aux molécules d'eau alors que les sel anhydre les molécules ne sont attachées à aucune molécule d'eau. Nous appelons ces molécules d'eau « eau de cristallisation ».
A savoir aussi, comment se forment les sels hydratés ?
Hydrate de Sels . Lorsque sels cristalliser à partir d'une solution aqueuse, les ions peuvent retenir une partie des hydratant molécules d'eau et former les hydrates solides tels que Na2CO3·10H2O et CuSO4·5H2O. La taille de l'ion et sa charge contrôlent l'étendue de hydratation.
Qu'arrive-t-il à un sel hydraté lorsqu'il est chauffé?
Lorsqu'un hydrater le sel Est chauffé , la structure cristalline du composé va changer. De nombreux hydrates donnent de gros cristaux bien formés. Ils peuvent se briser et former une poudre lorsque l'eau d'hydratation est chassée. La couleur du composé peut également changer.
Conseillé:
Quel est le nom du sel formé par la neutralisation de l'acide chlorhydrique et de la soude ?
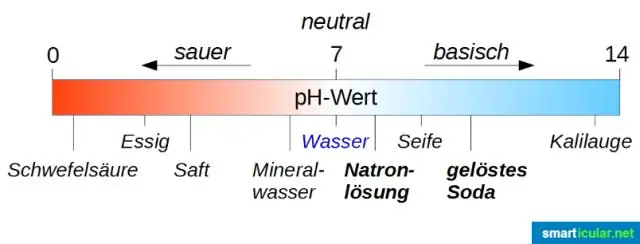
Explication : La réaction entre l'hydroxyde de sodium (NaOH) et l'acide chlorhydrique (HCl) est une réaction de neutralisation qui entraîne la formation d'un sel, de chlorure de sodium (NaCl) et d'eau (H2O). C'est une réaction exothermique
Quel est le pourcentage massique d'eau dans l'hydrate CuSO4 5h2o ?

Une mole de CuSO4•5H2O contient 5 moles d'eau (ce qui correspond à 90 grammes d'eau) dans sa structure. Par conséquent, la substance CuSO4•5H2O est toujours constituée de 90/250 ou 36% d'eau en poids
Combien d'eau y a-t-il dans l'hydrate?

MESURE EXPÉRIMENTALE DU POURCENTAGE D'HYDRATATION : La différence entre les deux masses est la masse d'eau perdue. La division de la masse d'eau perdue par la masse d'origine d'hydrate utilisée est égale à la fraction d'eau dans le composé. Multiplier cette fraction par 100 donne le pourcentage d'eau dans l'hydrate
Que se passe-t-il lorsqu'un sel hydraté est chauffé ?

Lorsqu'un sel hydraté est chauffé, la structure cristalline du composé change. De nombreux hydrates donnent de gros cristaux bien formés. Ils peuvent se briser et former une poudre lorsque l'eau d'hydratation est chassée. La couleur du composé peut également changer
Quelle est la formule du sel hydraté ?

1 Le sel inorganique s'hydrate sous forme de MCP. Les hydrates de sel constituent un groupe important de MCP. Un sel inorganique hydraté (sel hydraté ou hydrate) est un composé ionique dans lequel un certain nombre de molécules d'eau sont attirées par les ions et donc enfermées dans son réseau cristallin. La formule générale d'un sel hydraté est MxNy
