
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
L'unicité de Carbone
Parce que chaque carbone est identique, ils ont tous quatre électrons de valence, ils peuvent donc facilement se lier avec d'autres carbone atomes pour former de longues chaînes ou anneaux. En fait, un carbone l'atome peut se lier avec un autre carbone atome deux ou trois fois pour faire des liaisons covalentes doubles et triples entre deux carbone atomes.
De même, on peut se demander, qu'est-ce qui est unique à propos de l'élément carbone ?
Carbone est le seul élément qui peut former autant différent composés parce que chacun carbone atome peut former quatre liaisons chimiques avec d'autres atomes, et parce que le carbone l'atome est juste ce qu'il faut, de petite taille pour s'intégrer confortablement en tant que parties de très grosses molécules.
Aussi, quels sont les 5 faits intéressants sur le carbone ? Faits intéressants sur le carbone
- Environ 20% du poids des organismes vivants est du carbone.
- On connaît plus de composés qui contiennent du carbone que n'en contiennent.
- Le diamant est un excellent abrasif car c'est le matériau commun le plus dur et il a également la conductivité thermique la plus élevée.
D'ailleurs, quelles sont les deux propriétés uniques du carbone ?
Nature polyvalente de Carbone . Mais qu'est-ce qui fait Carbone un élément aussi intéressant peut être directement attribué à son deux propriétés uniques , c'est-à-dire tétravalence et caténation. C'est à cause de ces Propriétés que l'élément a la capacité de former un grand nombre de composés.
Pourquoi le carbone est-il spécial en chimie organique ?
Chimie organique études carbone contenant des molécules et le composés elles forment. Carbone est spécial car il peut s'attacher à quatre autres atomes, et il peut le faire de différentes manières, des anneaux aux chaînes, en passant par les doubles ou même les triples liaisons.
Conseillé:
En quoi le technétium est-il unique ?

Le technétium est l'élément radioactif le plus léger du tableau périodique et ses isotopes se désintègrent en une variété d'autres éléments, dont le ruthénium stable. Le grand avantage du technétium-99m (demi-vie de six heures) est qu'il est produit par désintégration de l'isotope molybdène-99 à vie beaucoup plus longue (demi-vie de 67 heures)
En quoi la transduction est-elle unique ?
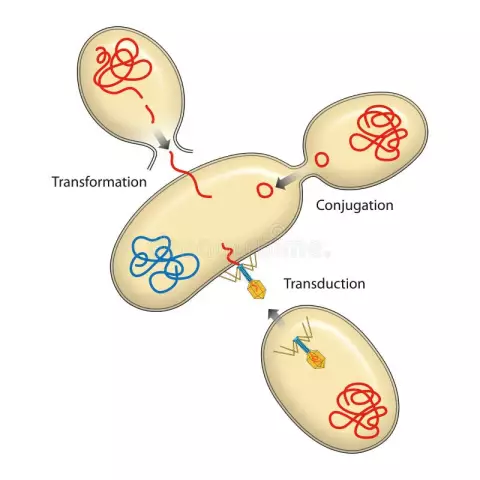
En quoi la transduction est-elle unique par rapport à une infection bactériophage normale ? Le bactériophage ne sort pas d'une cellule infectée pendant la transduction. La transduction transfère l'ADN du chromosome d'une cellule à une autre. Le bactériophage emporte avec lui des fragments de la cellule lors de la transduction
En quoi le graphite est-il unique ?

Si vous êtes une personne d'esprit scientifique, les propriétés du graphite vous intéresseront. Le graphite a un point de fusion à la pression atmosphérique, est un bon conducteur de chaleur et résiste à de nombreux produits chimiques, ce qui en fait un matériau idéal pour les creusets
Quel est le pourcentage (%) en masse de carbone dans le monoxyde de carbone CO) ?

% massique C = (masse de 1 mol de carbone/masse de 1 mol de CO2) x 100. % massique C = (12,01 g / 44,01 g) x 100. % massique C = 27,29 %
En quoi le Ring of Fire est-il unique ?

Faits sur le Cercle de feu Le Cercle de feu a longtemps été un site actif pour les tremblements de terre et les volcans en raison des limites actives des plaques. Lorsque les plaques tectoniques se déplacent les unes contre les autres aux limites, elles provoquent des tremblements de terre et des éruptions de magma, qui se transforment en volcans
