
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Dernière modifié 2025-01-22 16:58.
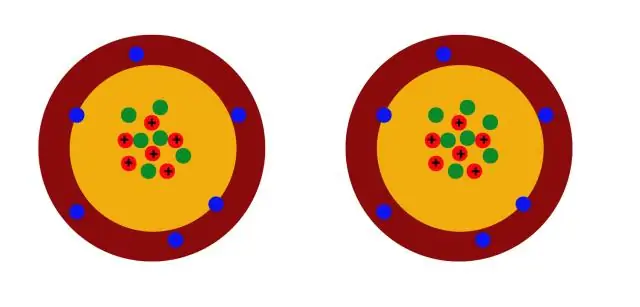
Isotopes d'un élément partagent le même nombre de protons mais ont des nombres de neutrons différents. utilisons carbone par exemple. Il ya trois isotopes de carbone trouvé dans la nature - carbone -12, carbone -13, et carbone -14. Tous les trois ont six protons, mais leurs nombres de neutrons - 6, 7 et 8, respectivement - diffèrent tous.
À ce propos, pourquoi le carbone 12 est-il un isotope ?
1 réponse. Parce que l'élémentaire carbone a plusieurs isotopes . Tous carbone noyaux possèdent 6 protons, mais certains carbone les noyaux possèdent plus de 6 neutrons.
Par la suite, la question est de savoir comment se forment les isotopes du carbone ? Naturel isotopes C est produit par les neutrons thermiques du rayonnement cosmique dans la haute atmosphère et est transporté vers la terre pour être absorbé par la matière biologique vivante.
De cette manière, pourquoi le carbone 14 n'est-il pas considéré comme un isotope ?
Parce que les atomes ont toujours la même quantité de protons et de neutrons. Ils ont tous le même numéro atomique, le même nombre de protons. Expliquer pourquoi carbone - 14 et l'azote- 14 sommes non considérés comme des isotopes l'un de l'autre ? Car ce sont deux éléments différents.
Qu'est-ce qui fait de quelque chose un isotope ?
Les atomes d'un élément chimique peuvent exister sous différents types. Ceux-ci sont appelés isotopes . Ils ont le même nombre de protons (et d'électrons), mais des nombres de neutrons différents. Différent isotopes du même élément ont des masses différentes. La masse est le mot pour la quantité de substance (ou de matière) quelque chose a.
Conseillé:
Le carbone 12 est-il un isotope radioactif ?

Le carbone, par exemple, a trois isotopes naturels : 12C (carbone-12), 13C (carbone-13) et 14C (carbone-14). C est radioactif et émet des rayons bêta qui ont été utilisés pour la mesure des poussières respirables, mais sa concentration dans le charbon est faible, de l'ordre de 1 × 10&moins;10 % dans le dioxyde de carbone atmosphérique
Comment la structure du carbone est-elle liée à la variété des macromolécules présentes dans les êtres vivants ?
L'atome de carbone a des propriétés uniques qui lui permettent de former des liaisons covalentes avec jusqu'à quatre atomes différents, ce qui rend cet élément polyvalent idéal pour servir de composant structurel de base, ou « colonne vertébrale » des macromolécules
Qu'est-ce qu'un isotope et comment est-il utilisé en datation radiométrique ?

La datation radiométrique est une méthode utilisée pour dater les roches et autres objets sur la base du taux de désintégration connu des isotopes radioactifs. Le taux de désintégration fait référence à la désintégration radioactive, qui est le processus par lequel un noyau atomique instable perd de l'énergie en libérant un rayonnement
Comment le carbone 14 est-il mesuré ?
Il existe trois techniques principales utilisées pour mesurer la teneur en carbone 14 d'un échantillon donné : le comptage proportionnel au gaz, le comptage à scintillation liquide et la spectrométrie de masse par accélérateur. Le comptage proportionnel au gaz est une technique de datation radiométrique conventionnelle qui compte les particules bêta émises par un échantillon donné
Quel est le pourcentage (%) en masse de carbone dans le monoxyde de carbone CO) ?

% massique C = (masse de 1 mol de carbone/masse de 1 mol de CO2) x 100. % massique C = (12,01 g / 44,01 g) x 100. % massique C = 27,29 %
